Características del ácido sulfúrico
Entre las principales características que pueden ser observadas en el ácido sulfúrico se mencionan las siguientes:
- Es un producto que se obtiene a partir del SO2 o dióxido de azufre.
- Se le conoce también con el nombre de tetraoxosulfato (IV), tetraoxosulfúrico (VI), aceite de vitrolio o licor de vitrolio.
- Se puede encontrar en diferentes tipos de presentaciones y su pureza puede variar de forma considerable.
- Se forma naturalmente gracias a la oxidación de los minerales conocidos como sulfuros que se encuentran en las rocas.
- Es un tipo de ácido diprótico.
- Es una sustancia considerada como peligrosa por su elevado nivel de irritación y corrosividad que puede provocar.
Historia
Los orígenes del ácido sulfúrico se pueden remontar al siglo VIII gracias a Jabir ibn Hayyan. Posteriormente, el ácido fue más estudiado en el siglo IX por Ibn Zakariya al-Razi, quien era un alquimista. En la Europa medieval, fue conocido con el nombre de aceite de vitrolio, una palabra que tenía como significado “cristal” y que era usada para referirse al aspecto que tenían las sales de sulfato.
Ya para el siglo XVII, Johann Glauber, un químico alemán-holandés, logró producir el ácido sulfúrico como tal, cuando mezcló nitrato de potasio con azufre en un medio con vapor. En 1763, Joshua Ward, un farmacéutico de Londres, usó este mismo método para empezar a producir el producto en masa. Ya para el siglo XVIII, luego de varios intentos por producir mayores cantidades, se logró hacer un proceso de destilación en seco por medio de la quema del disulfuro de hierro con sulfato de hierro a una temperatura de 480°, lo que daba como resultado ácido sulfúrico en cualquier concentración. En el año 1831, se logró patentar un proceso mejor y más rápido para producir ácido sulfúrico gracias a Peregrine Phillips, y hasta el momento, este es el método que se utiliza.
Estructura
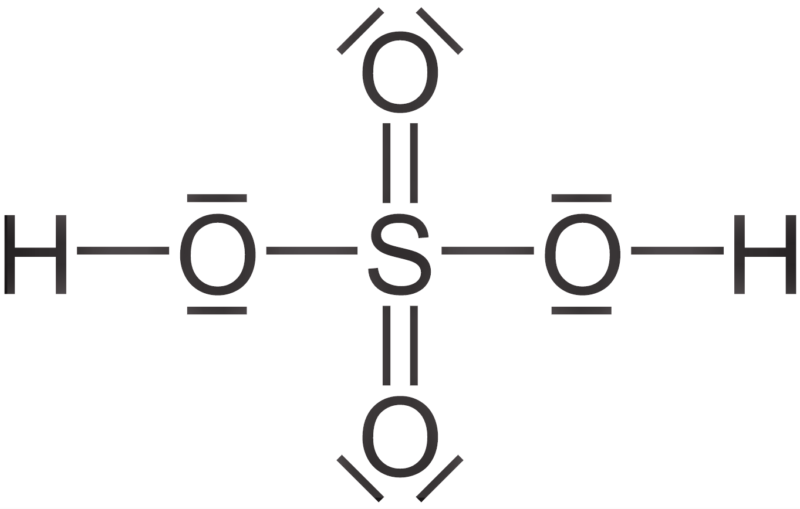
La estructura del ácido sulfúrico es piramidal. Cuenta con un átomo de azufre que se localiza en la parte central y los átomos de oxígeno se encuentran ubicados en cada uno de sus vértices y las dos restantes partes corresponden a los átomos de hidrógeno.
Fórmula
Su fórmula química estándar es H2SO4 lo que indica que en el compuesto se pueden encontrar dos átomos de hidrógeno, un átomo de azufre y cuatro átomos de oxígeno.
Nomenclatura
La nomenclatura del ácido sulfúrico se encuentra en los tres tipos de nomenclatura que existen, éstos son:
- Nomenclatura sistemática: en este tipo de nomenclatura se conoce con el nombre de tetraoxosulfato (VI) de hidrógeno.
- Nomenclatura stock: en ella se le nombra como ácido tetraoxosulfúrico (VI).
- Nomenclatura tradicional: su nombre es establecido como ácido sulfúrico.
Propiedades físicas del ácido sulfúrico
Las principales propiedades físicas del ácido sulfúrico son las siguientes:
- Es un líquido que tiene una consistencia de tipo aceitosa y además, tiene un olor muy particular, similar a los huevos cuando están en estado de descomposición, el cual también depende de la concentración del producto.
- Tiene un punto de fusión que se ubica en los 10° C.
- Su punto de ebullición se da en 337° C.
- Posee una densidad de 1,84 g/cm3.
- Cuenta con un peso molecular de 98,08 g/mol.
- Tiene una gravedad específica de 1,841; 100%.
Propiedades químicas
Entre sus principales propiedades que pueden ser encontradas en el ácido sulfúrico son las siguientes:
- El ácido sulfúrico es un oxidante muy fuerte.
- Puede disasociarse en el agua en proporciones bajas y altas.
- Cuando se encuentra concentrado y además caliente, se vuelve una sustancia muy oxidante y puede incluso atacar a los metales preciosos.
- Puede descomponer las sales de otros ácidos.
- Tiene propiedades higroscópicas gracias a la formación de los hidratos.
- Es un material combustible en sí mismo y también tiene la capacidad de poder iniciar la ignición de otras sustancias combustibles.
- Puede reaccionar de forma violenta en presencia de materiales reductores.
- Es un corrosivo para varios tipos de metales y produce durante el proceso, humos de dióxido de azufre y de hidrógeno gaseoso.
Obtención
Al ácido sulfúrico puede ser creado en diferentes tipos de concentraciones y grados de pureza. Dos son los principales métodos por los cuales se puede llegar a producir este tipo de ácido:
- Método de cámaras de plomo: este es el mecanismo más antiguo y se usa cuando se necesita producir ácido que será usado posteriormente en la fabricación de productos fertilizantes. Consiste en un método de diluido en donde el dióxido de azufre se oxida y luego se disuelve en el agua. El calentamiento se produce en un reactor que se conoce con el nombre de Torre de Glover.
- Método de contacto: este tipo de método de producción es capaz de generar mayor pureza en el ácido y mayores niveles de concentración. Para poder realizar este método se necesitan sustancias puras y catalizadores que resultan ser bastante costosos. En este proceso, el ácido sulfúrico es producido por un proceso de hidratación, una mezcla de gases secos que contiene aproximadamente un 7% de SO2 y un 14% de O2, los cuales se precalientan para luego depurare al máximo.
Usos del ácido sulfúrico
El uso principal que se le da a este tipo de ácido es en la industria petroquímica y química, principalmente en la producción de fertilizantes y en los procesos de refinación del petróleo, fabricación de explosivos, plásticos y detergentes. En cuanto a los fertilizantes, su uso se basa en la producción de ácido fosfórico y algunas pocas cantidades son también utilizadas para producir sulfato de amonio y superfosfatos.
En cuanto a la industria petroquímica, el ácido sulfúrico es utilizado principalmente como un medio de reacción por el cual se pueden realizar diferentes tipos de procesos orgánicos como condensaciones, nitraciones y deshidrataciones. Se utiliza en la producción del ácido fluorhídrico y clorhídrico y en varios procesos relacionados con al industria maderera como la fabricación de fibras químicas y procesos textiles.
Beneficios
Sus principales beneficios se presentan en el campo de la industria, específicamente en la química pues es un producto necesario para poder crear diferentes tipos de químicos. Es capaz de descomponer químicamente hablando muchos materiales y resulta ser una buena fuente de ingresos para los países en donde se produce.
Riesgos
El ácido sulfúrico concentrado es extremadamente corrosivo y puede causar graves quemaduras cuando no se manipula adecuadamente. Este producto químico, además de producir quemaduras químicas, produce quemaduras térmicas secundarias como consecuencia de la deshidratación que también produce. Este peligroso producto químico es capaz de corroer la piel, papel, metales e incluso la piedra. Si entra en contacto directo con los ojos, puede causar ceguera permanente. Si se ingiere, puede producir quemaduras internas, daños orgánicos irreversibles y la muerte.
La exposición a aerosoles que contienen ácido sulfúrico en altas concentraciones puede llegar a ocasionar una grave irritación de los ojos y en las vías respiratorias así como daños en los tejidos. Cuando esta exposición se da de forma constante incluso a bajas concentraciones, puede ocasionar la erosión de los dientes de una persona. Cuando se utiliza en los hogares, es común que se haga para limpiar los desagües, este tipo de ácido tiene los mismo efectos dañinos por lo que se deberán seguir las instrucciones correctas para su uso y para así evitar posibles riesgos.