Definición
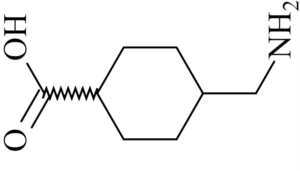
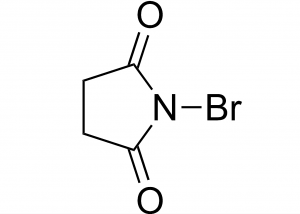
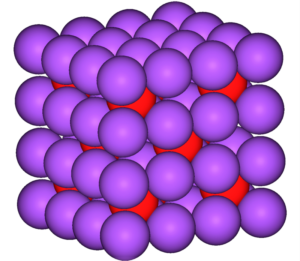
Un compuesto químico es toda sustancia compuesta por dos o más átomos de tipología diferente. Posee una estequiometria en una proporción fija. Goza de una distribución química exclusiva y precisa. Su unión se debe a la disposición espacial especificada por enlaces químicos.
Hay compuestos de tipo molecular, que permanecen unidos por enlaces covalentes, sales que se mantienen entre sí por uniones iónicas, y combinaciones intermetálicas conservadas juntas por enlaces metálicos. También subgrupos conservados en unión por lazos covalentes ordenados.
Características de los compuestos químicos
Las características de los compuestos químicos varían según sean estos orgánicos o inorgánicos:
Orgánicos
- Su estado es líquido o gaseoso.
- Son insolubles en agua.
- Tienen conductividad aislante.
- Su punto de fusión es bajo.
Inorgánicos
- Su estado es sólido.
- Son solubles en agua.
- Son conductores en solución y fundidos.
- Tienen un alto punto de fusión.
Origen
Todo elemento químico se ha formado en el interior o fondo de los planetas y estrellas, gracias a complicadas transformaciones y procesos de licuación y fisión atómica. Estas metamorfosis generan elementos bastante pesados por medio de un proceso conocido como núcleosíntesis. Y es así como se supone que se ha originado toda la materia del cosmos. A excepción de aquellos elementos que el hombre ha inventado o creado por sí mismo. Estos han sido originados en laboratorios o con el apoyo de reactores nucleares.
Historia
La definición de sustancia química se instituyó sólidamente en el siglo XVIII. El químico Joseph Proust ejecutó un trabajo relacionado con la estructura de ciertos químicos puros. Del mismo obtuvo como conclusión que toda muestra de un compuesto tiene la misma estructura, e igual mesura, en masa, de las sustancias que lo componen.
Lo mencionado anteriormente se conoce como Ley de composición constante. El avance de los métodos de compilaciones en la química orgánica, el hallazgo de numerosos elementos químicos y las nuevas técnicas en el área de la investigación, produjeron el nacimiento de la química actual.
Clasificación
De acuerdo al tipo de enlace químico, los compuestos químicos se dividen:
- Moléculas fusionadas en enlaces covalentes.
- Agregados inter metálicos conciliados por enlaces metal, suelen ocurrir en átomos del tipo férreo.
- Mezclas iónicas unidas por alianzas electromagnéticas y dotadas con carga negativa o positiva.
- Compuestos que mantienen unidos sus alargadas estructuras, a través de enlaces covalentes sistematizados.
Por su composición, se dividen:
- Compuestos inorgánicos: Son los que no tienen que ver con la vida. Se congregan entre sí con formas diferentes, obedeciendo a propiedades esenciales de la biósfera. A su vez se clasifican en:
- Hidróxidos: Se forman por la reacción de un óxido básico y el agua, caracterizada por mostrar el grupo oxidrilo.
- Óxidos básicos: Llamados también óxidos metálicos, lo forman un metal y oxígeno.
- Hidruros: De origen metálico o no metálico. Compuesto por un componentes e hidrógeno.
- Óxidos ácidos: Además citados como óxidos no metálicos. Lo conforman un no metal y oxígeno.
- Oxisales: Se forman por la reacción de un oxácido y un hidróxido.
- Hidrácidos: Son hidruros no metálicos que, cuando se disuelven en agua, adquieren carácter ácido.
- Sales binarias: Compuestos formados por un hidrácido más un hidróxido.
- Oxácidos: Aquellos derivados de la unión de un óxido ácido con el agua. Las moléculas quedan desarrolladas en un no metal, oxígeno e hidrógeno.
- Compuestos orgánicos: Su elemento base es el carbono, y en torno a él se constituyen los demás. Son los compuestos fundamentales, para la química de la vida. Pueden ser:
- Polímeros: Macro moléculas, resultado de la unión de moléculas chicas conocidas como monómeros.
- Aromáticos: Es un combinado cíclico fusionado, poseedor de gran estabilidad, por su deslocalización electrónica en relaciones pi.
- Alifáticos: Son compuestos orgánicos creados con carbono e hidrógeno, no son aromáticos.
- Órganos metálicos: Los átomos de carbono crean uniones covalentes, conllevan electrones, con átomos metálicos.
- Heterocíclicos: Son agregados orgánicos constantes donde al menos uno de los elementos del ciclo es distinto al carbono.
Tipos de compuestos químicos
Se conocen cuatro tipos, que obedecen a la manera en que están unidos los átomos que lo forman:
- Moléculas fusionadas por enlaces covalentes.
- Compuestos iónicos formados por enlaces iónicos.
- Compuestos intermetálicos fusionados por enlaces metálicos.
- Determinadas mezclas que se conservan unidas por alianzas covalentes ordenadas.
Propiedades
Inorgánicas: Son derivados de procesos naturales o por la intrusión humana en el laboratorio. Se forma regularmente por reacciones químicas. Intervienen impulsos de naturaleza química y física como sublimación, fusión y otras. En general carecen de carbono.
Orgánicas: Poseen compuestos de carbono. Son causados por el ser vivo (moléculas coligadas a individuos vivos).
Formación
Los compuestos químicos están desarrollados por un mínimo de 2 elementos. Estos han accionado entre sí y producido otra sustancia distinta a los componentes originarios. Existen tres tipos de enlaces que un compuesto puede tener: Iónico, covalente y metálico. Forma de los compuestos:
- Orgánicos: Desarrollados por enlaces covalentes (enlaces de dos átomos no metálicos). Poseen una combinación de enlaces carbono e hidrogeno. Destacan más átomos como el nitrógeno, oxígeno y azufre.
- Inorgánicos: Se forman por enlaces iónicos y covalentes, es decir, un no metal y un metal. Carece de enlaces carbono-hidrógeno.
Fórmula
Los científicos representan los compuestos con símbolos químicos de los átomos conectados. La fórmula da información del aporte de los átomos. Se utilizan abreviaturas regladas de los elementos y subíndices que muestran la cantidad de átomos incluidos. Es así como la fórmula del agua (H2O), indica que está compuesta por dos átomos de hidrógeno y uno de oxígeno.
En cuanto al orden de los elementos en la fórmula, con los inorgánicos se coloca el más electronegativo a la derecha. En la fórmula del cloruro de sodio (NaCl), el cloro es el más electronegativo. Los compuestos orgánicos constan de otras reglas donde emplean fórmulas esqueletales o semiavanzadas para formularlos.
Importancia
Su importancia radica en que intervienen en innumerables aspectos de la vida humana entre los cuales destacan:
- La industria de alimentos: En ella estudia el procesamiento de los alimentos einterviene en la nutrición.
- En la medicina: Tiene como fin identificar las síntesis y el adelanto de nuevos compuestos químicos que sean apropiados en el uso terapéutico.
- Minería: Lacomposición química es muy importante para poder diferenciar los minerales. Con este fin se efectúan exámenes químicos cualitativos y cuantitativos. Igualmente es de utilidad para determinar la simetría de los cristales.
Ejemplos de compuestos químicos
Es muy fácil encontrar ejemplos frecuentes de compuestos químicos:
- En el hogar: El agua (H2O), hidróxido de sodio o sosa caustica (NaOH), comercializado como lentejas, escamas o perlas. El azúcar o sacarosa (C12H22O11). El aceite. La sal (NaCl). Bicarbonato de sodio (NaHCO3) y el vinagre, dilución de ácido acético (C2H4O2).
- En la medicina, ciertos medicamentos son de composición sencilla, como el yodo, el agua oxigenada y bicarbonato de sodio. Existen igualmente medicamentos como antibióticos, antipiréticos, antiinflamatorios y analgésicos.
- Inventados por el hombre, destacan el azúcar, la mantequilla, detergentes, cloro, agua oxigenada, vinos, champoo y otros.
Más peligrosos: Destacan: Amianto, causante de cáncer. Arsénico, muy tóxico. Benceno, causa cáncer y anemia. Cadmio, toxico daña riñonesy sistema óseo. Flúor, el exceso provoca fluorosis del esmalte y huesos. Mercurio, bastante toxico para la salud humana.