Características del óxido de etileno
El óxido de etileno fue preparado por primera vez en el año 1859 por el químico francés Charles-Adolphe Wurtz, quien logró obtenerlo tratando el 2-cloroetanol con una base. Fue un producto de gran importancia industrial durante la Primera Guerra Mundial como precursor del refrigerante etilenglicol y del arma química conocida como gas mostaza. Entre sus características más sobresalientes se mencionan las siguientes:
- Tiene la importante función de actuar como un reactivo para formar diferentes productos, principalmente plásticos y polímeros.
- Tiene la capacidad de poder dañar las moléculas de ADN.
- Es un gas que se caracteriza por ser muy inflamable.
- Su aspecto es incoloro.
- Tiene un olor muy similar al éter.
- Tiene un peso mayor que el del aire.
- Puede ser soluble en agua y en la mayor parte de los disolventes de tipo orgánico que existen.
- Se presenta de forma comercial como gas licuado luego de que es licuado a presión atmosférica y a una temperatura determinada.
- También se conoce como epoxietano, oxirano y óxido de dimetileno.
Estructura
La estructura del óxido de etileno tiene forma de un anillo con tres miembros. Es un tipo de estructura triangular y forma ángulos de enlace de 60° por lo que se considera que éstos enlaces son débiles. Su estructura se muestra a continuación:
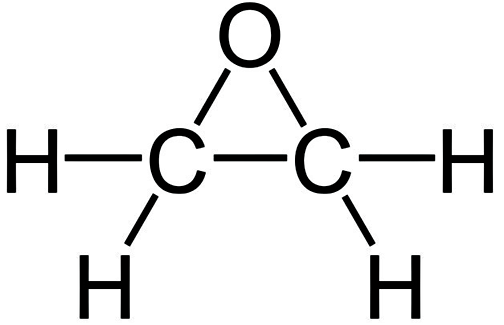
Fórmula
Su fórmula química es la siguiente: C2H4O.
Nomenclatura
En cuanto a su nomenclatura, el nombre dado por la IUPAC es el de Oxirano.
Propiedades físicas del óxido de etileno
Entre sus principales propiedades físicas se mencionan las siguientes:
- El óxido de etileno cuenta con un peso molecular de 44,1.
- Encuentra su punto de ebullición cuando se somete a una temperatura de 10,7º C.
- Su punto de fusión se puede encontrar en los -112º C.
- Posee además un punto de inflamación el cual se encuentra en los < -18º C.
- El óxido tiene también una temperatura de autoignición la cual logra alcanzar cuando llega a los 429º C.
- Cuenta con una densidad relativa (agua=1) de 0,88.
- Su densidad de vapor es de 1,5.
- Es un óxido soluble en agua.
Propiedades químicas
En cuanto a sus características químicas, el óxido de etileno tiene la propiedad de tener un poder de reacción bastante elevado principalmente cuando se mezcla con álcalis y con ácidos, cuando esto sucede, adquiere un enorme poder de explosión pues tiene la capacidad de crear un tipo de reacción exotérmica. Cuando se encuentra en su estado líquido, puede llegar a polimerizarse con gran facilidad, y en este proceso, desprende grandes cantidades de calor lo que hace que su riesgo de explosión también se vea aumentado.
Puede también ser descompuesto en otros productos como propano, etano, hidrógeno, acetaldehído y monóxido de carbono cuando se encuentra en presencia de calor. Reacciona también de forma violenta cuando se encuentra en presencia de algunos productos como el alcohol, el amoníaco y los oxidantes fuertes.
Obtención
El óxido de etileno se fabrica en grandes industrias capacitadas para su producción. En la actualidad, el proceso que se utiliza para poder obtener el óxido de etileno se realiza por medio de la oxidación de forma directa del etileno por medio de una corriente de oxígeno y catalizadores de plata. El oxígeno que se utiliza en el proceso debe de ser obtenido en una planta dedicada al fraccionamiento del aire. Además, el catalizador debe de contar con al menos 15% de su peso en plata, la cual se coloca en un soporte inerte y poroso de alúmina.
El tipo de reacción que se utiliza para poder obtener este óxido es exotérmico con una entalpía y con la reoxidación del óxido de etileno a dióxido de carbono y agua. Normalmente, también se incluyen modificadores químicos durante el proceso de obtención como por ejemplo, el cloro. Las presiones utilizadas para la reacción son del orden de 1-2 MPa y la ecuación química que se utiliza para poder crear esta reacción es:
H2C=CH2 + ½ O2 → C2H4O
La reacción anteriormente mencionada se realiza por medio de un producto intermedio, en este caso el oxametalacíclico, el cual además da lugar a dos posibles vías de reacción:
- Formación de óxido de etileno: H2C=CH2 + O → C2H4O
- Formación de acetaldehído: H2C=CH2 + O → CH3CHO (este es el primer paso para poder completar la completa produciendo al mismo tiempo dióxido de carbono y agua.
Además, puede producirse en los laboratorios químicos gracias a la acción de un hidróxido alcalino (OH-) sobre la clorhidrina de etileno siguiendo la fórmula que se menciona a continuación:
CH2OH-CH2Cl + OH- → C2H4O + Cl- + H2O
Usos del óxido de etileno
El uso principal que se le da al óxido de etileno es el de intermediario en la producción de varios tipos de productos químicos, como por ejemplo, productos anticoagulantes, para diversas aplicaciones industriales y para la creación de productos de consumo diario, como por ejemplo los limpiadores domésticos, artículos de cuidado personal y tejidos y textiles. Una muy pequeña cantidad de este óxido es también utilizado para la fumigación y para la esterilización.
Sus derivados son de suma importancia dentro del campo de la industria, por ejemplo, le etilenglicol, un producto que posteriormente se puede transformar en fibras de poliéster las cuales se utilizan para fabricar productos de tapicería y alfombras. Este producto también se usa para que funcione como un refrigerante, para la producción de fibra de vidrio y como un anticongelante en los vehículos.
El gas de óxido de etileno tiene la capacidad de eliminar las bacterias, el moho y hongos. Por eso se puede utilizar para esterilizar sustancias que resultarían dañadas por técnicas como la pasteurización, que se basan en el calor. Se utiliza ampliamente en pequeñas cantidades para esterilizar suministros médicos como vendas, suturas e instrumentos quirúrgicos. Además, resulta muy funcional para poder obtener esteres acéticos los cuales son luego utilizados como un monómeros de plásticos vinílicos.
Ventajas
Además de las grandes ventajas que ofrece al campo de la industria, el óxido de etileno tiene también otras ventajas las cuales están ligadas a los procesos de esterilización, éstas se mencionan a continuación.
- Logra propagarse de forma correcta y eficaz en los pliegues y en los lugares que son de difícil acceso, garantizando de esta forma una correcta esterilización.
- Puede esterilizar los productos a una temperatura relativamente baja lo que garantiza que los objetos no pierdan su forma ni que se destruyan.
- Puede atravesar con mucha facilidad los envoltorios de los productos que se quieren esterilizar.
- Tiene una eficacia máxima para poder esterilizar los productos que son considerados como termosensibles ya que éstos no tiene la capacidad de poder ser esterilizado utilizando métodos convencionales que funcionan mayormente con vapor de agua.
Riesgos
El óxido de etileno es considerado como un contaminante ambiental y además, como un peligroso tóxico para los seres humanos. De hecho, varios estudios han demostrado que tiene la capacidad de aumentar el riesgo de padecer varios tipos de cáncer, principalmente cuando la exposición al óxido de hace de forma crónica. En los lugares donde se trabaja con este tipo de material, el equipo y traje de seguridad es necesario y se han establecido además una serie de normas para controlar las emisiones del mismo en la atmósfera.
Cuando se inhala, puede producir graves daños en el sistema respiratorio. Es un depresor importante del sistema nervioso central y cuando se inhala puede producir infecciones y en casos graves edemas pulmonares. Mareos, vómitos, dolores de cabeza y diferentes tipos de trastornos nerviosos pueden presentarse luego de su exposición. Al entrar en contacto con la piel puede producir irritaciones en la piel y si la exposición es grave, se pueden producir quemaduras con necrosis tisular.
Es un producto que puede provocar una importante irritación en los ojos e incluso también puede provocar quemaduras en estos órganos, dolor y visión borrosa son síntomas comunes. Si el producto se ingiere, se puede absorber de forma muy rápida lo que hace que ocasione daños en los riñones e hígado.