Características del óxido de cobre
Entre las características más representativas que pueden ser encontradas en el óxido de cobre se mencionan las siguientes:
- Era conocido anteriormente con el nombre de óxido cúprico.
- Puede ser encontrado en algunas rocas de la superficie terrestre en forma de mineral el cual se conoce con el nombre de mineral cuprita.
- Es un compuesto semiconductor de estructura monoclínica.
- Es un óxido de tipo metálico.
- Se encuentra formado por un átomo de cobre y por un átomo de oxígeno.
- Es un compuesto que tiende a ser muy irritante porque está por lo general disuelto en diferentes ácidos minerales.
- Existen dos tipos de óxidos de cobre, el I que es encontrado en las rocas de color ojo y el II que posee un número de oxidación mucho mayor y en este caso se conoce con el nombre de tenorita.
Estructura
El óxido de cobre posee un tipo de estructura iónica por lo que tiene fuerzas de atracción electrostática entre sus iones. La interpretación gráfica de su estructura se muestra a continuación:
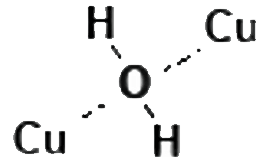
Fórmula
Su fórmula básica es Cu2O.
Nomenclatura
En cuanto a la nomenclatura del óxido de cobre, ésta puede realizarse de tres maneras distintas:
- Nomenclatura sistemática: en la cual se le conoce como monóxido de dicobre.
- Nomenclatura stock: en donde se llama óxido de cobre (I).
- Nomenclatura tradicional: conocido también como óxido cuproso.
Propiedades físicas del óxido de cobre
Sus propiedades físicas más importantes se detallan a continuación:
- Tiene un color rojizo o amarillo el cual depende principalmente del tamaño que tengan sus partículas. En el caso del óxido de cobre II, puede tener una apariencia de polvo de color negro.
- No es soluble cuando está en contacto con el agua pero puede ser soluble cuando está en presencia de una solución de amoníaco.
- El óxido de cobre tienen una densidad de 6,0 g/cm3.
- Su masa molar se ubica en los 143,09 g/mol.
- Cuenta con un punto de fusión de 1235 °C.
- Su punto de ebullición se ubica en los 1800 °C.
- No es considerado como un compuesto inflamable.
- Es normalmente estable incluso en condiciones de altas temperaturas.
Propiedades químicas
Entre sus propiedades químicas se encuentran las siguientes:
- Tiene la capacidad de producir HCuCl2 cuando se disuelve en ácido clorhídrico.
- Es anfótero, en otras palabras, no puede ser disuelto en los ácidos o en soluciones alcalinas.
- El óxido de cobre II es muy venenoso y tóxico cuando se ingiere.
- Es muy estable en seco y en condiciones atmosféricas normales.
- Puede adherirse fuertemente a los minerales y a la materia orgánica.
- Reacciona con ácidos para formar sales de cobre.
Obtención
En el caso del óxido de cobre I, éste puede llegar a ser obtenido a partir del mineral conocido como cuprita el cual se encuentran en las rocas de color rojizo, además, puede formarse en piezas de cobre que han sido chapadas en plata y que luego se exponen a la humedad para que produzca un tipo de corrosión. En cuanto al óxido de cobre (II), éste se puede obtener de cuatro maneras distintas, las cuales son:
- Calentamiento de nitrato de cobre (II): 2 Cu + O2 →2 CuO
- Calentamiento de carbonato de cobre (II): CuCO3 →CuO + CO2
- Calentamiento de hidróxido de cobre (II): Cu(OH)2 (s)→CuO (s) + H2O (l)
- Por combustión directa del cobre en presencia de aire: 2 Cu(s) + O2(g) →2 CuO(s)
Usos del óxido de cobre
Como se mencionaba con anterioridad, existen dos tipos de óxidos de cobre. En el caso del óxido de cobre I, puede ser utilizado como un tipo de pigmento con el cual se pueden elaborar esmaltes de color rojo, gris, negro y verde. Es también uno de los componentes principales en la producción de hidróxido de cupramonio el cual se usa para fabricar rayón. Es usado también en el campo de las ciencias como un tipo de suplemento nutricional para animales que tienen déficit de cobre. Es un potente fungicida y es un buen semiconductor. En el campo de la agricultura puede ser usado para follaje como un humectante. Además, forma parte de los ingredientes que son utilizados en la creación de plaguicidas agrícolas.
El óxido de cobre tipo II, se utiliza principalmente para la aleación del cobre, para fabricar esmaltes y como un medio para eliminar diferentes tipos de materiales peligrosos por ejemplo el cianuro. En el campo de la agricultura también es utilizado como un tipo de fungicida. Es un componente básico en la fabricación de cristales y cerámicas. Ha sido usado también como un cátodo en la elaboración de pilas húmedas.
Un uso interesante del óxido de cobre se da en los barcos pues es usado como un tipo de agente anti incrustante para evitar con él la posible formación de percebes y de otros tipos de organismos marinos que pueden aferrarse en los fondos de los barcos y ocasionar problemas serios en la estructura de los mismos. Es utilizado también como un preservante de maderas, techos, tejas y en paredes que se encuentran en la orilla de los mares o acantilados.
Riesgos
Los óxidos de cobre tienen a ser peligros y potencialmente tóxicos, principalmente en el caso del óxido de cobre II el cual puede incluso provocar graves problemas en el sistema nervioso central y en el sistema endocrino. Son muy irritantes para las mucosas como los ojos y nariz y además pueden producir serios daños en el tejido epitelial. Si es ingerido, puede producir una depresión importante en los nervios, ocasionar graves problemas gastrointestinales, daños al hígado, a los riñones, al sistema vascular e incluso al sistema circulatorio.
Cuando se inhala, los pulmones sufren daños importantes y puede producir una condición médica conocida como “fiebre del humo metálico” el cual produce una serie de síntomas similares a los de una gripe. La dermatitis es otro problemas común que se da cuando las personas están expuestas a este tipo de óxido. Cuando la exposición se hace de forma prolongada y continua, se puede generar la aparición de la Enfermedad de Wilson. Por estas razones, el uso y la manipulación del óxido de cobre debe de hacerse bajo estrictas medidas de seguridad, en ambientes que no estén cerrados por completo y que por el contrario tengan una buena ventilación.