Características del ácido fosfórico
El ácido fosfórico es un líquido que tienen una serie de características. Algunas de ellas son las siguientes:
- No tiene color ni tampoco tiene olor.
- Evita el desarrollo de moho y bacterias en los refrescos.
- Se utiliza en muchas ocasiones como un aditivo en alimentos procesados.
- Se usa para mantener la frescura de las bebidas.
- La recomendación dada por los expertos de salud para que el cuerpo funcione adecuadamente es de 700 mg por día.
- Se puede encontrar por lo general en bebidas que presentan un color oscuro.
- Se puede encontrar comúnmente en la sal que se utiliza para la cocina.
- Es considerado como un tipo de sustancia química corrosiva.
- Puede presentarse en estados físicos o químicos pero esto dependerá de la temperatura a la que sea sometido y la pureza.
- Sus siglas en el Sistema Internacional de Numeración es de E-388.
Estructura
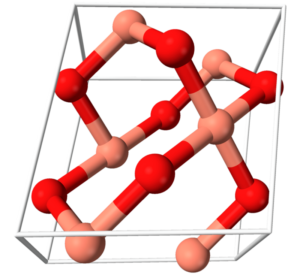
La estructura del ácido fosfórico se basa en un enlace P:O y tres P-OH. Los últimos enlaces son los que portan los hidrógenos liberados cuando están en un medio de disolución. El átomo de fósforo se localiza en el centro y el resto de los oxígenos forman una especie de tetraedro molecular.
Fórmula
La fórmula química del ácido fosfórico es la siguiente: H3PO4.
Nomenclatura
La nomenclatura de este ácido depende de las sales ternarias de los oxoácidos y, debido a que el átomo de P posee una valencia de +5, al ácido se le cola el sufijo –ico al prefijo fosfor-.
Propiedades físicas del ácido fosfórico
Sus principales propiedades físicas son:
- Cuando se encuentra a temperatura ambiente se presenta en forma de sustancia cristalina.
- Puede ser almacenado y transportado en forma de solución.
- Tiene una densidad relativa en agua de 1.68.
- Su masa molar es de 97,99 g/mol.
- Aunque no es inflamable cuando está en contacto con metales puede liberar hidrógeno el cual sí es explosivo.
- Cuando está en estado sólido puede tener forma de cristal ortorrómbico, higroscópico y además es transparente.
Propiedades químicas
Entre las principales propiedades químicas que pueden ser encontradas en el ácido fosfórico se mencionan las siguientes:
- Es un mineral que tiene tres átomos de hidrógenos, cuatro átomos de oxígeno y un solo átomo de fósforo.
- Tiene una densidad relativa de 1,83.
- Su punto de fusión se encuentra en 42,35° C.
- Su punto de ebullición es de 213° C.
- Tiene un pH de 1.5.
- Puede ser soluble cuando se expone al agua caliente aproximadamente 548 g/100 ml.
- Tiene una presión de vapor de 4 Pa a 20° C.
- Tiene la capacidad de corroer metales ferrosos y aleaciones.
- Junto a los metales puede reaccionar y formar hidrógeno gaseosos altamente inflamable.
- Se descompone cuanto está en contacto con alcohol, cianuro, cetonas, sulfuros y compuestos halogenados.
- Cuando se quema produce cantidades considerables de vapores tóxicos.
- En estado sólido tiene una densidad de 1,892 g/cm cúbico.
- Posee una viscosidad de 3,86 mPoise.
Obtención
El ácido fosfórico se encuentra normalmente en alimentos como la carne, los frijoles, el pescado y el huevo. Muchos alimentos que se consumen y que son enlatados en fábricas, incluyen en sus ingredientes este tipo de mineral. También puede fabricarse por medio de una serie de procesos térmicos o húmedos y en estos casos, el resultado que se obtiene es usado principalmente en la producción de fertilizantes. La principal y mayor fuente de donde se puede obtener el ácido fosfórico es la apatita, un mineral fosfatado.
Usos del ácido fosfórico
El ácido fosfórico es un mineral que puede ayudar a la adecuada formación de huesos y dientes, brinda apoyo a la función de los riñones en dosis adecuadas y recomendadas por un médico y también hace que los músculos del cuerpo puedan tener una recuperación mucho más rápida luego de que éstos hayan sido expuestos a entrenamientos pesados. Es también uno de los componentes fundamentales en la formación del ADN y ARN, códigos de suma importancia para los seres vivos.
Puede ser utilizado para eliminar el óxido de los metales cuando éstos se corroen.
Riesgos
En el cuerpo humano es común encontrar fósforo y por esa razón, no necesita que ingrese al organismo grandes cantidades del mineral, sin embargo, muchas personas lo toman sin control y sin el visto bueno de un médico y esto puede ocasionar una serie de problemas de salud. Una ingesta excesiva de ácido fosfórico podría llegar a producir diferentes tipos de complicaciones del corazón y podrían también aumentar el riesgo en las mujeres principalmente de padecer osteoporosis.
En altas dosis, tiene la capacidad de interferir de forma negativa sobre otros tipos de minerales como el magnesio y el hierro ocasionando otros tipos de patologías peligrosas como la anemia. Cuando está en contacto con otras sustancias químicas, puede resultar tóxico, causar irritación en la piel y afectar de forma considerable el sistema respiratorio.
Muchas personas acostumbran a ingerir altas dosis de refrescos carbonatados por día, y éstos incluyen en sus ingredientes ácido fosfórico. Al ser tomadas constantemente, el nivel del mineral aumenta de forma considerable en el cuerpo ocasionando que los riñones no los puedan eliminar adecuadamente y esto podría dañar éstos órganos en determinado momento. En casos extraños, cuando se encuentra en forma de rocío, puede producir irritación nasal y de garganta, dolor en el pecho y problemas respiratorios. Dependiendo de la concentración que tenga, al entrar en contacto con la piel podría provocar lesiones tisulares o quemaduras graves.
Impacto ambiental
Cuando el ácido fosfórico entra en contacto con el ambiente se transporta por medio del aire en forma de neblina. Esta neblina posteriormente es depositada en el suelo y algunos de sus minerales, principalmente los carbonatos se mantiene libre alcanzando el manto freático y contaminando las aguas. Cuando esto sucede, se produce toxicidad para los peces acabando con la vida acuática y destruyendo plantas de ríos.