Características del ácido clórico
Las características más sobresalientes del ácido clorhídrico son las siguientes:
- Es un oxidante bastante potente.
- Tiene un peso molecular de 84.45914 g/mol.
- Cuenta con una densidad de 1 g/mol.
- No tiene color, en otras palabras, es incoloro.
- Se caracteriza por ser un compuesto corrosivo cuando está en presencia de telas o metales.
- Es un tipo de compuesto bastante inestable.
- Es peligroso para los seres vivos pues es también muy irritante.
- Puede mantenerse estable cuando está en una solución acuosa.
- Puede ser sintetizado en los laboratorios de forma directa a partir de sus sales.
- Se conoce también con el nombre de Trioxoclorato (V) de hidrógeno.
Estructura
La estructura del ácido clórico se muestra a continuación:
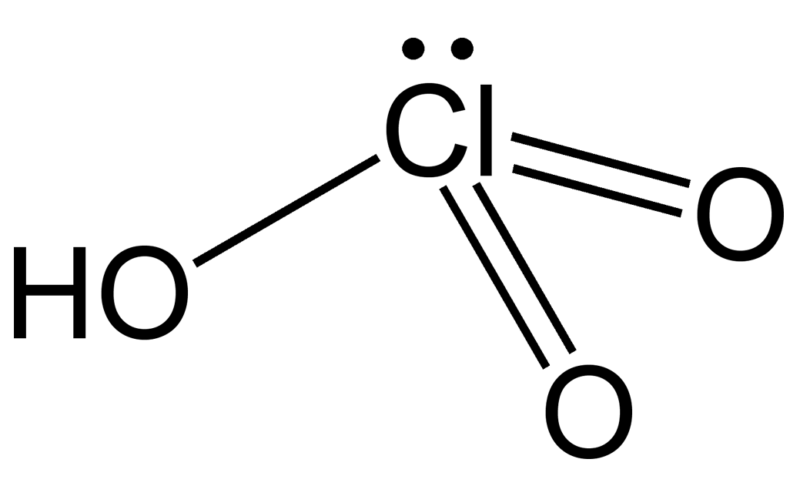
Fórmula
Está formado por un átomo de cloro, un átomo de hidrógeno y tres átomos de oxígeno. Dos átomos de oxígeno unidos al átomo de cloro tienen doble enlace y el tercer átomo está unido con un enlace simple. La fórmula química o molecular para representar esta estructura química es HClO3.
Nomenclatura
La nomenclatura para este tipo de ácido es la siguiente:
- Nomenclatura sistemática: se conoce con el nombre de trioxoclotato (V) de hidrógeno.
- Nomenclatura stock: llamado ácido trioxoclórico (V).
- Nomenclatura tradicional: conocido como ácido clórico.
Propiedades físicas del ácido clórico
A continuación se mencionan sus principales propiedades físicas.
- Este ácido solamente puede encontrarse en forma de solución.
- No tiene olor ni tampoco tiene un aroma que lo caracterice.
- Tiene una densidad de 1g/ml a 25 °C.
- Su punto de ebullición se encuentra en los 100° C.
Propiedades químicas
Entre sus principales propiedades químicas mencionamos las siguientes:
- El ácido clórico tiene la propiedad de ser un oxidante bastante fuerte y tiene incluso la capacidad, cuando está en altas concentraciones, de iniciar el fuego en materiales orgánicos.
- Es un ácido bastante fuerte también y reacciona con bases para poder formar sales de clorato.
- Puede desproporcionarse dando origen a una gran variedad de productos como el ácido perclórico, dióxido de cloro y oxígeno.
- Se comporta de forma estable cuando está en soluciones acuosas frías.
- Tiene una acidez de −1 pKa.
- Posee un punto de ebullición de 313,15 K (40 °C).
- Su punto de fusión es de 253,15 K (−20 °C).
Obtención
La obtención del ácido clórico se puede realizar siguiendo dos mecanismos diferentes:
- Por medio del clorato de bario con ácido sulfúrico que producen finalmente sulfato de bario por medio de la reacción química: Ba(ClO3)2 + H2SO4 → 2HClO3 + BaSO4.
- Por medio del calentamiento del ácido hipocloroso para poder obtener el ácido clórico siguiendo la reacción química que se detalla a continuación: 3HClO → HClO3 + 2HCl.
- Otro método de síntesis del ácido clórico es el calentamiento del ácido hipocloroso para producir ácido clórico junto con cloruro de hidrógeno.
Usos del ácido clórico
El principal uso que se le da al ácido clórico es en la formación de sales de clorato, calcio, magnesio, plomo, cobre, plata y otros. Es un reactivo que también es usado para eliminar metales pesados en el aire que tengan un alto nivel de toxicidad, por ejemplo, el mercurio elemental. Es utilizado también como un agente oxidante y como catalizador en la polimerización del acrilonitrilo. Cuando se combina adecuadamente con otros ácidos y productos es funcional en las labores de limpieza pues es un potente desinfectante, antibacterial y depurador.
En este caso, cuando se usa como limpiador, es utilizado para remover las impurezas que se acumulan en los utensilios de cocina pues cuando éstos son sumergidos en agua con el ácido, la suciedad y corrosión se desprende. Es también usado en los tratamientos de las aguas residuales pues funciona muy bien eliminando materias orgánicas y microorganismos nocivos presentes en este tipo de agua.
En el campo de la industria, el ácido clórico se utiliza gracias a las diferentes sales que puede producir y para generar otros tipos de compuestos como el protocloruro de mercurio, un compuesto utilizado para la fabricación de luces de bengala. Funciona también como un tipo de bactericida para el control de las plagas de gusanos que se originan en algunos cultivos. Con él también se puede fabricar cloruro de vinilo, material necesario para la fabricación de las tuberías PVC.
Riesgos
El ácido clórico es un agente oxidante poderoso y por esta razón, su ingesta, inhalación o contacto con la piel es un peligro para la salud. Los vapores de este tipo de ácido pueden llegar a provocar lesiones graves en todo el sistema respiratorio que pueden incluso provocar la muerte. Cuando se quema, el humo que despide se convierte en un gas bastante irritante, corrosivo y además tóxico. También puede ocasionar graves daños en los riñones y en las mucosas del cuerpo humano.