Definición
El término es utilizado principalmente dentro del campo de la física y se refiere a la cantidad de calor que es necesario para poder hacer que una determinada sustancia logre aumentar su grado de temperatura en unidades de grado Celsius. Es el calor específico el que se encarga de poder determinar la cantidad de energía que consume el agua por cada grado centígrado que logre hacer que la temperatura aumente.
Características del calor específico
Entre las principales características que podemos encontrar en el calor específico se mencionan las siguientes:
- Por lo general puede ser medida en grados Celsius.
- Es considerada como una propiedad intensiva de la materia.
- Es también conocida con el nombre de capacidad térmica específica o capacidad calórica específica.
- Puede llegar a variar dependiendo del estado de la materia en el que se encuentre la sustancia.
- Mide la cantidad de energía que es necesaria para poder provocar un aumento en la temperatura.
- Es totalmente independiente de la masa que se tenga.
- La cantidad de energía que absorbe la sustancia se debe de expresar en Joules.
Cómo se calcula el calor específico
Para calcular el calor específico que se expone a una temperatura determinada (T) se hará el siguiente procedimiento:
c = lim (Δt→0) . Q / m.ΔT = 1/m . dQ/dT
Formula
La fórmula más utilizada para poder determinar el calor específico de una sustancia es la siguiente:
ĉ = Q / m.Δt
en donde:
- Q: se encarga de representar la transferencia de calor que se da entre el sistema y el entorno.
- M: se refiere a la masa de la sustancia o materia.
- Δt: es la variación que posee la temperatura a la cual la materia es sometida.
Unidades de medida
Las unidades de medida del calor específico se encuentran dentro del Sistema Internacional de mediciones y se utiliza la unidad de calor que es representado con el símbolo J o Joules por kilogramo y por kelvin. En algunas ocasiones puede ser medido por medio de las calorías por gramo o también por grados centígrados. En algunos países se mide utilizando BTU´s por libra y Fahrenheit.
Para qué sirve
El calor específico sirve para poder entender y conocer la cantidad de calor que se debe de aplicar en un cuerpo determinado para poder elevar la temperatura del mismo. Es un aspecto de mucha importancia para poder realizar cálculos sobre los posibles efectos del calor en los materiales de construcción que forman parte de los hogares y edificios.
En qué se diferencia de la capacidad calorífica
La capacidad calorífica o térmica es el cociente que existe entre la cantidad de energía calorífica que es transferida hacia un cuerpo por medio de cualquier proceso y está relacionada con el cambio en la temperatura que éste experimenta. Se puede decir que es la energía que se necesita para poder elevar la temperatura de una sustancia. El calor específico por su parte, es una magnitud física, que define la cantidad de calor que puede ser suministrada a una sustancia para poder elevar la temperatura.
Importancia
El calor específico juega un papel de suma importancia en el campo de las ciencias pues cumple la importante función de poder elevar la temperatura para lograr de esta manera una correcta descomposición de las moléculas que poseen los elementos, con el objetivo principal de poder separar y analizar cada una de las partículas que la conforman.
Algunos tipos de composiciones orgánicas son bastante reactivos al calor y por esta razón pueden llegar a cambiar su textura y su tamaño, gracias al calor específico es posible entonces lograr alcanzar niveles exactos para una correcta desintegración o evaporación cuando se necesita realizar algún tipo de intervención química.
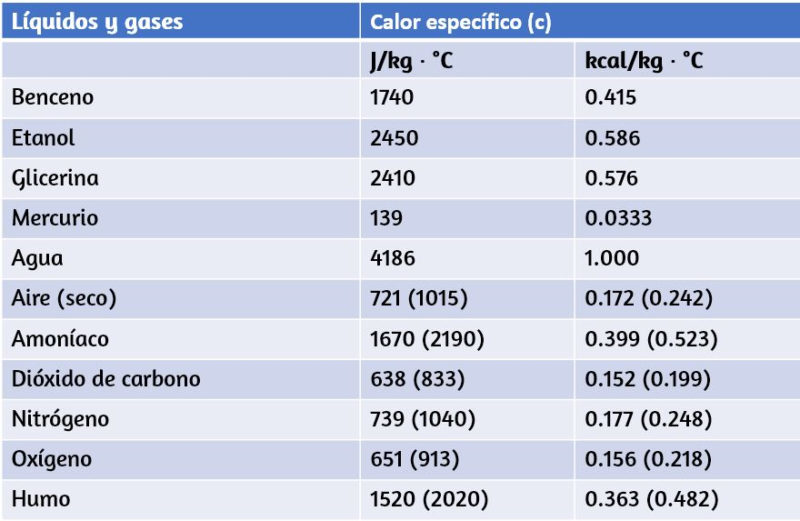
Tabla
A continuación se muestra un ejemplo de tabla para calor específico:
Otros ejemplos de calor específico
- Calor especifico del cobre: 0,385 (J/ g·K)
- Calor específico del aluminio: 0,900 J/ºC·g.
- Del vapor de agua: 2,01 kJ/ (kg·K) 0,48 cal/ (g·°C)
- Del aire: 1,003 J/ºC·g
- Del hielo: 2,090 J/ºC·g.
- Calor específico del plomo: 0.0305 calorías por gramo.
- Calor específico del hierro: 0,444 J/ºC·g.
- Del acero: 460 J / (kg * ° C)
- De la madera: 0.41 calorías por gramo.
- Del nitrógeno: 1040 J (Kg·K)
- Calor especifico del hidrogeno: 14.310 calorías por gramo por grados Celsius
- Calor especifico de la plata: 0,234 J/ºC·g.
- Del zinc: 390 J/(Kg·K)
- Del etanol: 3,79 kJ/(kg·K)
- De la leche: 0.93 – 0.94 cal/gºC