Definición
El calor latente es el tipo de calor que se presenta cuando una sustancia no varía su temperatura aunque esté ante una energía térmica, sin embargo, logra modificar el estado de segregación. Es una magnitud de tipo física que logra brindar información sobre la cantidad de energía térmica o calor que una sustancia necesita para poder ser capaz de recibir o de perder calor con el objetivo de cambiar su estado. Esto implica que se de un cambio de sólido a líquido, de líquido a gaseoso y así sucesivamente.
Características del calor latente
Entre las principales características que pueden ser observadas en el calor latente mencionamos las siguientes:
- Produce cambios en el estado de la materia.
- No incrementa la temperatura que posee un determinado cuerpo.
- Es llamado también calor de evaporización.
- Forma parte del modelo conocido como teoría calórica.
- Es un tipo de calor que no puede ser sentido.
Tipos
Existen varios tipos de calor latente los cuales se mencionan a continuación:
- Calor latente de fusión: este tipo de calor se basa en la fusión el cual es un proceso físico que se da debido a la transición que sufre una sustancia cuando pasa del estado sólido al líquido. Entonces, éste tipo de calor latente puede ser definido como el cambio de entalpía que surge de la absorción de la energía lo cual puede provocar que la sustancia pase de una fase sólida a una líquida. Este proceso de da gracias a la temperatura de fusión y tiene una presión de 1 atm o 101 325 kPa.
- Calor latente de vaporización: se conoce con el nombre de entalpía de vaporización y se refiere a la cantidad de energía que necesita ser agregada a una determinada sustancia cuando ésta está en fase líquida para que pueda originarse la transición hacia la fase gaseosa. Se relaciona con el punto de ebullición de una sustancia.
- Calor latente de solidificación: se refiere al calor que está involucrado dentro del cambio de fase cuando una sustancia pasa del estado líquido al sólido. Es opuesto al calor latente de fusión porque la energía que se libera hacia la parte externa se produce cuando se genera el cambio de fase.
- Calor latente de condensación: se presenta en el momento en el que se da un cambio en una sustancia que pasa del estado gaseoso al líquido, por ejemplo el vapor de agua.
Cómo se calcula el calor latente
El calor latente puede ser calculado de forma exacta utilizando una fórmula en la cual se establece que el calor necesario para poder hacer que una determinada sustancia pueda cambiar de fase dependerá del tipo de cambio de fase que se pretenda.
Fórmula
Para poder hacer el cálculo del calor latente en una sustancia se utiliza la siguiente fórmula:
Q = m. L
Donde
- Q: se refiere a la cantidad de calor (cal o J)
- m: indica la masa (go kg)
- L: muestra el calor latente (cal / go J / kg)
Unidades
Las unidades que se utilizan para poder representar el calor latente se encuentran dentro del Sistema Internacional y se mide en Joules / Kilogramo (J/kg). También puede ser medido en algunas ocasiones utilizando las cal/g o calorías por gramo.
En qué se diferencia del calor especifico
La diferencia es que el calor específico es la cantidad de calor que debe de ser suministrada a la sustancia o sistema para que éste pueda aumentar la temperatura de la misma y que además depende del valor de la temperatura inicial. Por otro lado el calor latente es la energía que se necesita para poder hacer un cambio en la fase, en otras palabras, el paso de una sustancia de sólido a líquido o de líquido a gaseoso.
Importancia
La principal importancia del calor latente radica en la atmósfera de la Tierra puesto que es el factor principal que interviene de forma importante en la formación de las nubes de convección y además participa en mantener la estabilidad o la inestabilidad de la atmósfera.
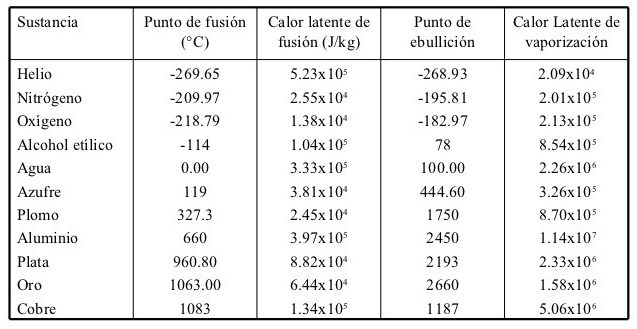
Tabla
A continuación se presenta un modelo de tabla de calor latente.
Otros ejemplos de calor latente
- Calor latente de vaporización: h lg = 2257 kJ / kg
- Del agua: 334·103 J/kg
- De la plata: de 105 kJ/kg.
- Calor latente del cobre: 214 /kg a 1.083 °C
- Del plomo: 2.45 J/kg
Calor latente de condensación
El calor latente de condensación se presenta en el momento en que se da el cambio de fase de una sustancia cuando pasa del estado gaseoso al líquido, por ejemplo, el proceso que se da en el vapor de agua. El valor que tiene el calor latente de condensación es el mismo que el de la vaporización, pero con la diferencia que tendrá un valor negativo. Es importante mencionar que, entre mayor temperatura se tenga, más se reducirá el calor de condensación y de la misma forma le punto de ebullición aumentará.